
【喜报】铭研医药完成pre-A轮融资,估值过亿!
2020年,对各行各业来讲都是不容易的一年!医药行业面临着前所未有的挑战,既要承受新冠疫情对业绩的冲击,又要经历国家政策调控的阵痛。在此严峻的形势下,铭研医药承受住重重考验,于近日顺利完成Pre-A轮融资,公司估值过亿。这标志着铭研医药的业务模式和发...
2020-12-28
【公司新闻】为这不平凡的2020,献上送别的《赞歌》
12月17日晚7点半,76岁的国宝级马头琴艺术大师齐·宝力高老师,率领世界第一支马头琴乐队——“野马”,在北京国家大剧院音乐厅,举办了一场震撼人心的新年音乐会。在公司组织下,北京铭研医药研究有限公司在京员工集体出席,共同度过了一个难忘的夜晚。
2020-12-21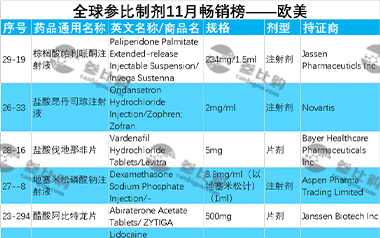
【排行榜】日本、欧盟、美国,11月,这些参比制剂最火爆!
11月日本,欧盟,美国热门的参比制剂
2020-12-01
【药研杂记】蛇毒研究进展:从致命毒素到新药开发
本文对一些主要蛇毒组分,蛇毒毒性效应及其解毒,蛇毒在肿瘤、心血管疾病、神经退行性疾病以及抗炎、抗菌、免疫调节、镇痛、抗病毒等方面的应用进行重点阐述。
2020-11-26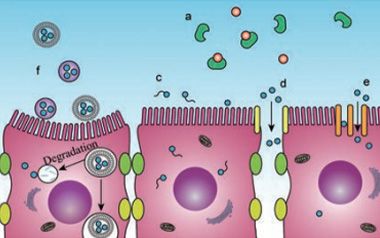
【药物制剂】为了做出口服胰岛素,有人开了这些脑洞……
本文综述了胃肠道中存在的吸收屏障,以及克服这些阻碍提高胰岛素口服生物利用度的策略,并对这些创新技术与材料的安全性及应用前景进行分析,以探讨胰岛素口服给药的可行性。
2020-11-26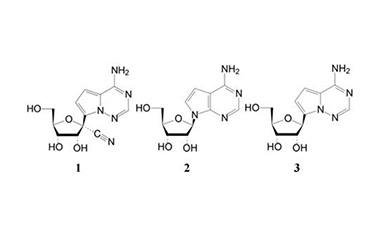
【药研分析】由同情用药发展为全球首个新冠疗法的瑞德西韦
本文对瑞德西韦的研发路径加以简要的介绍。
2020-11-25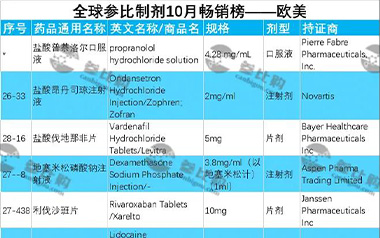
【排行榜】日本、欧盟、美国,10月,这些参比制剂最火爆!
10月日本,欧盟,美国热门的参比制剂
2020-11-25
【免费参会】“首届中国国际仿制药大会”100个免费VIP名额等你抢!
2021年3月,我们精心策划和筹备在北京召开“药仁汇2021北方(北京)峰会暨第一届中国国际仿制药发展大会”。会议共设置了五个部分:政策法规论坛;原辅料论坛;制剂论坛;质量分析论坛;临床研究论坛。会议内容以技术和实践为主,议题上更加关注制药新生代感兴...
2020-11-18
【药研说】生物创新药Vs化学仿制药,谁才是当世英雄?
看到这个标题,您也许会觉得一头雾水——这有可比性吗?的确,生物创新药和化学仿制药,虽然名字都是“药”,但在制药人看来,却属于完全不同的两个领域。它们在结构、成分、生产方法、研究方法、生产设备、知识产权、配方、保存方法、监管标准乃至商业模式上,都不一样...
2020-11-05
【药研新闻】最新!CDE《化学仿制药参比制剂遴选申请资料要求》重磅发布!
为更好地服务申请人,进一步提高参比制剂遴选工作的质量和效率,药审中心组织制定了《化学仿制药参比制剂遴选申请资料要求》(见附件),根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审核...
2020-10-23






