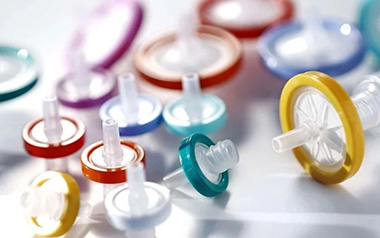
【药物分析】带新宝典,药研10年总结的样品前处理中滤膜选择方法
最近小编遇到一个事情很是恼火,刚刚购买的色谱柱,进样不到20针,主峰竟然分叉,不管如何洗脱都无法恢复。今天小编就来818滤膜的事情。为什么要拿这么简单的滤膜选择的事情出来讲,有一个至关重要的原因,哪个新手没有因为滤膜毁掉一次实验。。。
2019-05-21
【药研分析】HPLC法校正因子研究中的几个问题
PLC法具有将不同物质分离后逐一定量的分离分析能力,在药品有关物质检测中发挥着越来越重要的作用,成为药品杂质控制中常用而有效的手段之一。
2019-05-21
【药研分析】99个关于色谱柱的问题解答,你关心的都在这!(一)
关于色谱柱的99个问题,涉及色谱的很多方面,希望能给做药物分析的同仁提供一些帮助,由于文章较长,共分成五期发布,希望大家持续关注!
2019-05-16
【注射剂】30年经验国际专家讲解注射剂研发——曹家祥老师专访
昨天药研江湖推送了曹家祥老师关于溶出试验的问题解答, 今天继续带来曹老师关于注射剂问题的相关解答,也欢迎各位同仁留言讨论。
2019-05-15
【药物制剂】30年经验国际专家讲解溶出试验——曹家祥老师专访
4月,药研江湖参加了第九届仿制药峰会,有幸对国际知名制剂专家曹家祥老师进行了采访。
2019-05-14
【药研分析】我可真是个不让人省心的实验员啊~~你可别学我!
一个好的实验习惯不但能保证试验顺利,还能让试验者能事半功倍。不过总是有一些人呢,就是不让人省心!不但糟糕的试验习惯影响了自己,有时候还连累了别人!
2019-05-13
【药研趣闻】那个诞生无数伟大发明的实验室,一个世纪前是个什么样子呢?
“不是在实验室,就是在前往实验室的路上!”在很久很久以前,在那些简陋的实验室科学家们优势如何创造这个世界的呢。看到这些实验室历史图像一定会欣喜若狂,一个世纪前的实验室老照片,你可以看一个个的时代。
2019-05-13
【药物分析】搞懂色谱方法开发过程中流动相pH的确定
适用范围:本思路仅适用于反向色谱法分析离子化合物方法开发中流动相pH的确定。
2019-05-13
【药研技巧】梳理仿制药研发流程,讲解处方工艺研究内容
本期将对仿制药的研发流程进行简单讲解,一些内容由于政策要求变化会有不同,但是研发的流程基本思路没有变化!
2019-05-10
医药包装协会发布《药包材生产质量管理指南》,5月8日开始实施!
中国医药包装协会团体标准《药包材生产质量管理指南》(T CNPPA 3005-2019)已于2019年5月8日发布,自2019年5月8日起实施。
2019-05-09






