今天,国家药品监督管理局发布了《M4:人用药物注册申请通用技术文档》(以下简称M4)模块一文件:行政文件和药品信息。同时,国家药品监督管理局还发布了M4指导原则中文全文。
通告明确说明自2019年7月1日起,对2018年第10号公告规定情形的药品注册申请,申请人应按照M4模块一文件要求提交资料。
提示:关注公众号:药研江湖 后台回复“CTD文档”,下载整理好的附件文件。
依据原食品药品监管总局《关于适用国际人用药品注册技术协调会二级指导原则的公告》(2018年第10号)(以下简称2018年第10号公告)有关规定,国家药品监督管理局组织制定了《M4:人用药物注册申请通用技术文档》(以下简称M4)模块一文件:行政文件和药品信息,现予以发布。自2019年7月1日起,对2018年第10号公告规定情形的药品注册申请,申请人应按照M4模块一文件要求提交资料。
同时,国家药品监督管理局组织翻译了M4指导原则全文,形成了中文版,一并予以发布。
特此通告。
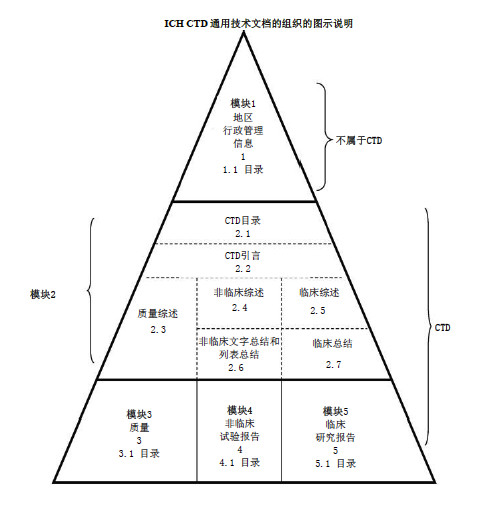
附件:《M4:人用药物注册申请通用技术文档(CTD)》模块一文件及CTD中文版
国家药监局
2019年4月11日
附件部分文件预览:


声明:药研江湖对所有公众号产生内容保持严谨、中立的态度。文章仅供交流学习使用。如遇到内容有误,请与我们联系进行讨论和修改。(010-65104668)








