本出版物《经过治疗等效性评价批准的药品》(该目录即广为人知的橙皮书)在《联邦食品、药品及化妆品法案》(法案)的指导下,由美国联邦食品与药物管理局(FDA)在安全性与有效性的基础上对药品进行了认定。仅基于安全性而被批准上市销售的药品(涵盖了正在接受药品效力研究实施[DESI]审查的药品[如颠茄生物碱和利眠宁胶囊等]或1938年之前的药品[如镇静安眠剂药片等])并不包括在本出版物中。药品包含物质的主要评判标准是,该药品的批准申请有效,且该申请从未因安全性或有效性而被撤回。通过行政和司法对药品的限制,所列出的药品成分不受任何目前法规的约束。此外,该目录包含了对已批准的多源处方药品的治疗等效性的评价。这些评价将用于向各州保健机构、处方医师、药剂师提供公共信息及建议,以推动药品选择领域的公共意识及培养对保健成本控制的意识。本出版物中所涉及的治疗等效性评价并非是在法案指导下对药品的法律地位产生影响的官方FDA行为。
本出版物发行背景。 事实上,每个州都制定了法律或法规来鼓励药物替代品,以达到控制药品成本的目的。各州的法律均要求这些替代品或为特定目录中的限定药品(积极的处方药典)或适用于除特定目录中禁止的药品(消极的处方药典)以外的所有药品。根据上世纪七十年代末期请求FDA援助的积极和消极处方药典的需求数量,FDA显然不可能仅根据单一标准为每个州提供服务。FDA也认为,提供基于通用标准的单一目录,即可在不同定义及不同州的法律标准的基础上对药品进行评价。于是,1978年5月31日,美国食品与药物管理委员会给每个州的行政长官发出了一封信函,陈述FDA愿意提供一份目录,该目录涵盖FDA依据安全性及有效性而批准的所有处方药,以及对多源处方药的治疗等效性评价。
橙皮书于1979年1月被作为一份提案分发到各州。它仅包含了在法案的505条款指导下通过新药申请(NDA)和简化新药申请(ANDA)由FDA批准的上市销售处方药。
橙皮书中的治疗等效性评价反映了基于法案的505条款批准的多源处方药的具体标准。以代表评价基础的代码字母的形式表示这些评价。关于这些代码的详细内容可参阅“序言”。
美国FDA治疗等效性评价原则的背景及基础的充分讨论于1979年1月12日(44 FR 2932)发布在《联邦登记薄》上。包括了FDA对公众意见反馈的最终规则也于1980年10月31日(45 FR 72582)发布在《联邦登记薄》中。橙皮书的最终版本的第一版(1980年10月)包含了适当的修订及补充。随后每一版中均包含新的批准及数据的适当修改。
1984年9月24日,总统签署了药品价格竞争和专利恢复法案(1984年修正案)。1984年修正案要求FDA以每月积累增订的方式向公众发布获批药品目录。橙皮书的每月积累增刊满足这一需求。本出版物的附录认定那些1984年修正案的独占期限内有效的药品(在联邦法案505(b)(2)条款中规定的简化新药及其申请在特定时间段内不允许进行提交,除非许可,方可获得临时批准)并提供关于目录药品的专利信息,可能会延缓简化新药申请或505(b)(2)条款的批准申请。附录还提供额外信息,为向FDA提交新药申请的企业提供帮助。
FDA旨在利用本出版物以完善出版物的内容和评论以及相关的FDA程序。因此如果您有任何改善本出版物的建议,请发送至标签和项目协助室主管(MD20855 罗克韦尔市 斯坦迪什办事处7620 药品评价与研究中心 仿制药事务处 HFD-610)。我们收到的建议和评论将在信息公开法规的自由保证下进行公布。
橙皮书由四部分组成:(1)经过批准的具有治疗等效性评价的处方药品;(2)经过批准的非处方药(OTC),此类药品未包含于现有的OTC记录中,因此不通过新药申请或简化新药申请将无法上市销售;(3)在法案的505条款指导下,由生物评价及研究中心监管的批准药品;(4)获批药品累积列表,此类药品从未上市销售,或用于出口或军事方面,或已在市场上停止销售,或非安全性或有效性原因撤回申请而导致在市场上停止销售。1 本出版物还包含以商品名或确定的名称(如果商品名不存在时)及申请机构名称(获批申请的所有者)排序的处方药和非处方药的目录。活性成分的所有确定的名称均与(21 美国联邦法规汇编 299.4(e))中规定的官方药典名称或《美国采用药名》(USAN)保持一致。后者包含本出版物中缩写的申请机构名称。此外,还提供了一份统一术语的列表。
附录包含了处方药、非处方药品、停用药品目录及在法案的505条款指导下由生物评价和研究中心监管的药品专利与独占权信息。本出版物还包含FDA认为适合公布的额外信息。
在第六版之前,本出版物不包含非处方药及由生物评价和研究中心基于法案的505条款而批准的药品,其原因就是本出版物的主要目的在于为各州提供FDA推荐的信息,即选择药品时,仿制处方药也是可选项目。1984年修正案要求FDA发布所有上市贩售药品(非处方药及处方药)的最新目录,那些药品均因安全性和有效性以及其所需新药申请而获得批准。
在1984年修正案的指导下,一些药品获得临时批准。FDA不会将临时批准的药物包含在橙皮书中。临时批准的目录记载于简化新药申请(仿制药)。根据申请所有者随后的行为,临时批准变成完全批准时,FDA将在适当的获批药品目录中列出药品及最终批准期限。
橙皮书中的经销商或再包装者是不确定的。其原因就是经销商或再包装者将其货源供给者从一个获批制造商更换为另一个制造商时,他们并未被要求通知FDA,因此从经销该药品的经销商或再包装者获取完整药品批准信息几乎是不可能的。
药物等效药剂。如果药品包含相同的活性成分,剂型与给药途径相同,且具有相同规格或浓度(如盐酸利眠宁(5mg胶囊)),则它们被视为药物等效药剂。药物等效药剂被配制为具有相同剂型且包含相同剂量的活性成分,以满足相同、药典或其他适用标准(规格、质量、纯度及特性),但是它们在诸如形状、刻痕一致性、作用机制、包装、赋形剂(包括颜色、口味、防腐剂)、失效日期、特定限制、标示等特点上存在差异。除非在出版前橙皮书工作人员获得通知,根据配药需求(处方药或非处方药)或批准权,新获批药物将被添加至橙皮书的第1、2、3章节。
药物替代品。如果药品含有相同的治疗配基,但却包含不同的盐分、酯分或化合物成分,或不同的剂型或规格(如250mg的盐酸四环素胶囊 VS. 250mg的复合磷盐酸四环素胶囊;200mg的硫酸奎尼丁片剂 VS. 200mg的硫酸奎尼丁胶囊),则此类药品被视为药物替代品。通常FDA没有数据确定片剂与胶囊的生物等效性。缓释药品与相同活性成分的速释或标准释放配方比较时,单一制造商在一个产品线上制造的不同剂型及规格的药品为药物替代品。
治疗等效药剂。仅在药品具有药物等效性且在标示指定的条件下为患者配药时具有相同临床效果和安全性的情形下,此类药品被视为治疗等效药剂。
FDA认定满足下列通用标准的药品具有治疗等效性:(1)因安全性和有效性而被批准;(2)具有治疗等效性缘于(a)同一剂型和给药途径、且含有同等剂量的相同活性成分(b)符合规格、质量、纯度及药性的药典或其他适用标准;(3)具有生物等效性缘于(a)不存在已知或潜在生物等效性问题,且达到可接受的体外标准(b)如果存在已知或潜在问题,但却达到适当的生物等效性标准;(4)标示准确无误;(5)根据《现行优良制造规范》条例生产而成。治疗等效性的概念被用于完善橙皮书,仅适用于含有相同活性成分的药品,并不包含相同条件下的不同治疗剂的比较(例如,用于镇痛的盐酸丙氧芬与盐酸戊唑辛)。由非申请所有者重新包装和/或经销的药品均被视为与申请所有者的药品具有治疗等效性,即使申请所有者的药品为单一源或被编码为非等效性(如BN)。此外,申请所有者的药品的经销商或再包装者被视为与申请所有者拥有相同的代码。治疗等效性认定不适用于未经批准或未经临床试验的药品。
FDA认为达到上述标准的药品具有治疗等效性,即使药品在某些特性上有所不同,如形状、刻痕一致性、作用机制、包装、赋形剂(包括颜色、口味、防腐剂)、失效日期、标示的次要方面(如特定的药代动力学信息)及贮藏条件。护理一名特殊病人时这些差异就显得很重要,开药医师可能会根据医疗需要配制特定的专利药品。然而,FDA相信定义为具有治疗等效性的药品是完全有希望被取代,且替代药品与参比药物一样具有相同的临床效果和安全性。
生物利用度。该术语指的是从药品吸收活性成分或活性配基并产生效力的比率和程度。由于药品并不被血液吸收,因此可通过反映活性成分或活性配基产生效力的比率和程度来测定生物利用度。
生物等效药剂。该术语指的是在相似实验条件下研究时呈现出可类比的生物利用度的药物等效药剂或药物替代品。法案的505条款(j)(8)(B)解释了实验药物和参比药物(参阅1.4章)被视为生物等效药剂的条件:
在相似的实验条件(单剂量或多剂量)下配制相同剂量的治疗成分时,实验药物与参考药物的吸收比率和程度并未存在显著性差异;或者
在相似的实验条件(单剂量或多剂量)下配制相同剂量的治疗成分时,实验药物与参比药物的吸收程度并未存在显著性差异。与参比药物的吸收比率差异是有意为之,已反映至其提供的标示中,不是长期使用时的有效药物浓度达成的基本条件,以及被认为对药物没有太大的医学影响。
上述方法均不适用(如药品未被吸收到血液中)时,或许可使用其他体内或体外实验方法证明其生物等效性。
生物等效性有时可通过体外的生物等效性标准加以证明,特别是该体外实验与人体体内的生物利用度数据相关联时。在其他情况下,生物等效性有时也可通过临床比较试验或药效研究得以证明。
在1984年药品价格竞争和专利恢复法案的指导下,寻求批准上市的仿制药的制造商必须提交相关数据,以证明与先驱(原创性)药品具有生物等效性。1984年法案的前提就是生物等效药剂具有治疗等效性,因此具有可互换性。
生物利用度指的是从药品吸收活性成分或活性配基并产生效力的比率和程度(联邦食品、药品及化妆品法案的505条款(j)(8))。生物等效性指的是两种或两种以上药品或制剂中的同一药物的等同释放量。这将会从这些制剂中产生等量的吸收比率和程度。揭示生物等效性的概念是,如果一种药品含有一种化学性质相同的药物成分,且与另一种药品一样以相同的比率和程度传递到作用部位,则被视为等效且可替代的药品。可以在21 CFR 320.24找到用于定义生物等效性的方法,其中包括(1)药代动力学(PK)研究、(2)药效学(PD)研究(3)比较临床试验以及(4)生物体外研究。使用的研究以药物作用部位及研究设计的性能为基础,以比较两种药品可传递到作用部位的药物成分。
标准的生物等效性(PK)研究实施方法是,对一定数量的志愿者(通常为24至36名成年人)进行二次治疗交叉研究。同样也可以使用四期、重复设计交叉研究。配制单剂量的实验药物与参比药物,并在一段时间后测量药物的血液或血浆水平。揭示药物吸收比率和程度特性的药代动力学参数将被进行统计评价。行业的PK参数为血浆浓度-时间曲线(AUC)下面积,计算至最后的测试浓度(AUC(0-t))并将吸收程度推算至无穷尽(AUC(0-inf));以及将吸收比率推算为最大或峰值药物浓度(Cmax)。根据人体的长半衰期特点,药物的交叉研究可能不太好实现,因此可使用平行研究设计来代替。替代的研究方法(如体外研究或与临床或药效终端的等效研究)被用于药品,其原因是血浆浓度难以确定药物成分是否到达作用部位(如呼吸器、鼻喷剂和用于皮肤的局部用药)。
分析此类生物等效性研究的统计学方法被称为双单侧检验程序。下列两种情形均以此统计学方法来进行检验。第一种双单侧检验确定仿制药(实验药物)替代专利药品(参比药物)时是否呈现出明显更低的生物利用度。第二种双单侧检验确定专利药品(参比药物)替代仿制药(实验药物)时是否呈现出明显更低的生物利用度。根据FDA医学专家的观点,上述检验的差异高于20%时被确定为具有显著性差异,因此并非适用于所有药品。从数字上来看,这表示第一次统计检验的实验药物/参比药物的平均值极限为80%,而第二次统计检验的参比药物/实验药物的平均值极限为80%。按照惯例,对于实验药物/参比药物而言,所有数据均表示为平均反应率(AUC和Cmax),因此第二次统计检验的极限为125%(80%的倒数)。
基于统计学的缘由,所有数据都在统计检验之前进行了对数转换。实际上,这些统计检验均使用方差分析(ANOVA)和计算每个药代动力学参数(Cmax和AUC)的90%的置信区间来实施。药代动力学参数(AUC和Cmax)的置信区间必须全部位于上述80%至125%之间的范围内。由于研究数据的平均值位于90%的置信区间的中心,因此数据的平均值通常接近100%(实验药物/参比药物的比例为1)。通过临床比较试验的药效研究或体外比较方法证明生物等效性时,有时也会使用不同的统计标准。
上述生物等效性评价方法及标准同时控制实验药物与参比药物之间的平均反应差异,以及已推定的群体平均反应的精度。这种精度取决于两种药品的药代动力学参数(AUC和Cmax)的实验对象(普通志愿者或患者)以及研究的对象数量。90%置信区间的幅度为生物等效性研究中实验药物与参比药物的对象类型的反映。如果一种或两种药品的变异性较高且生物等效性研究的统计力度不足(如实验体数量不足),平均反应无差异的实验药物与参比药物进行比较时,仍有可能无法达到生物等效性标准。相反,平均反应存在较大差异的低变异性实验药物却可能会达到生物等效性标准。
仿制药的生物等效性评价系统确保了替代药品在体内性能方面基本上不会与参比药物存在太大差异。仿制药办公室进行了两次调查以确定仿制药和名牌药之间的差异。1985年和1986年间进行的第一次调查包含了获批申请中递交的224项生物等效性研究。参比药物与仿制药之间的AUC平均差异为3.5%(美国医学会杂志、1987年9月4日258卷第9号)。第二次调查包含了1997年批准的273项简化新药申请中递交至FDA的127项生物等效性研究。三项评审内容包括AUC(0-t)、AUC(0-inf)及Cmax。参比药物与仿制药之间的平均差异分别为,AUC(0-t) :+3.47% (SD 2.84)、AUC(0-inf):+3.25% (SD 2.97)以及Cmax:+4.29% (SD 3.72)(美国医学会杂志、1999年12月1日282卷第21号)。
监管的主要关注是使患者免受不具有生物等效性的药品的伤害。目前实施的双单侧检验保持在0.05等级的差异度,以确保未与参比药物具有完全等效性的仿制药获批的容错率不超过5%。
参比药物(2121 CFR 314.94(a)(3))指的是申请机构为该药品提出新药申请,且已获得FDA批准的药物。
FDA已经在处方药及非处方药目录中确定了那些与申请机构的药品的体内生物等效性(参比标准)及体外生物等效性比较的参比药物。FDA指定单一参比药物作为标准以使所有仿制药必须证明与其具有生物等效性,期望能避免仿制药与其参比专利药物可能存在的显著差异。仿制药与不同的参比药物进行比较时可能会出现这种差异。然而,在某些情况下目录药物被批准为单一药品时,未被指定为参比药物且未被证明与参比药物具有生物等效性的药品会避免仿制药竞争。一个公司希望在市场上销售未指定为参比药物的药品的仿制药时,可以通过公民请愿书的途径向FDA提出申请(详见联邦法规21 10.25(a)和联邦法规 10.30)。当公民请愿书获得批准时,第二目录药物将被指定为附加的参比药物,且申请机构可以提交一份引用指定参比药物的简化新药申请。满足必要生物等效性需求的“1.7章 治疗等效性评价代码”药品解释了同一类目的两种参比药物下列出的多源药品的代码系统(AB, AB1, AB2, AB3...)。
此外,两种情况下,两种被证明相互具有生物等效性的目录药物均可被指定为参比药物。第一种情况是生物等效性的体内确定不证自明且放弃体内生物等效性已获许可。第二种情况是两种目录药物的生物等效性可通过体外方法得以确定。在处方药和非处方药目录中通过“+”符号标示参比药物。此类标示的参比药物代表生物等效性的当前最佳判断。处方药和非处方药目录标示口服剂型、注射剂、眼部用药、耳部用药和局部用药的参比药物。我们建议,制药公司计划实施体内生物等效性研究,或计划制造要求放弃体内生物等效性的批次药品时,请与生物等效室、仿制药办公室联系以确认合适的参比药物。
橙皮书包含了公共信息和建议。它不会规定采购、开具、配制或替代哪种药品,也不会规定应该避免使用哪种药品。在某种程度上,橙皮书阐述了FDA对获批药品的治疗等效性的评价,它包含了FDA向公众、从业者及各州提出的药物选择建议。这些评价不会确定哪种药品违反了法案或哪种药品更优于其他药品。治疗等效性评价是基于证据的科学判断,而仿制替代药物可能会牵涉到各州制定的社会和经济政策,旨在减少消费者的药物成本。在某种程度上,橙皮书认定根据法案的505条款批准的药品,并发表FDA被要求公布的信息、以及公众根据信息自由法享有的知情信息。某种药品未包含在橙皮书中时,并不意味着该药品违反了法案的505条款,或该药品不具有安全性和有效性,或该药品与其他药品不具有治疗等效性。相反,这意味着FDA尚未对该药品的安全性、有效性及质量进行评价。
使用橙皮书时需要专业的管理和判断。 处方药的治疗等效性评价是由FDA基于科学和医学评价作出的。根据FDA的判断,FDA评价为具有治疗等效性的药品被期望具有相同的临床效果,且在标示条件下使用时的潜在副作用方面不存在差异。然而,这些药品在诸如形状、刻痕一致性、作用机制、包装、赋形剂(包括颜色、口味、防腐剂)、失效日期及标示等其他特性上可能会有所不同。具有上述差异的药品进行替代使用时,可能会因片剂的颜色和形状差异而引起患者的困惑,或因无适当的刻痕一致性而无法分片以提供指定剂量,或因口味而降低患者对某种药物的接纳程度。此外,对患者而言,在不利的贮藏条件下一种药物可能比另一种有更好的稳定性,或者极少情况下可能会因色料或防腐剂成分而出现过敏反应,以及在成本方面的差异。
FDA的治疗等效性评价不会降低从业者的职业责任感,他们会在开处或配制药品时向每一位患者履行应尽的责任及提供必要的信息。在那些情况下,治疗特殊患者时特定药品的特性而非其活性成分更重要时,有必要提供该药品的医嘱。药剂师还必须熟悉不同药品(特别是重制药品)的失效日期及贮藏的标示要求,以确保一种药品替代为另一种药品时向患者提供适当的建议。
多源和单一源药品。 FDA仅对在法案的505条款指导下批准的多源处方药作出治疗等效性评价,大多数情况下意味着那些治疗等效药剂由多家制造商提供。此类药品包含治疗等效性的代码,且以粗体显示药品信息并加注下划线。那些获得单一源药物批准申请的药品(仅有一种具有该活性成分、剂型、给药途径及规格的获批药品)也被包含在橙皮书中,但是此类药品不包含治疗等效性代码。由非申请所有者重新包装和/或经销的药品均被视为与申请所有者的药品具有治疗等效性,即使申请所有者的药品为单一源或被编码为非等效性(如BN)。此外,虽然没有在橙皮书中明确记载,申请所有者的药品的经销商或再包装者被视为与申请所有者拥有相同的代码。这些代码及定义原则的详细内容将在“1.7章 治疗等效性评价代码”中进行讨论。
橙皮书中列举的药品由获批申请所有者(申请机构)的名称来确认,但其未必是药品的制造者。申请机构可能已委托合同制造商制造其药品,或者仅经销获批的药品。然而,大多数情况下药品的制造商同时是申请机构。根据规定,制造商名称允许出现在标示中,即使该制造商并不是经销商。
虽然橙皮书中的药品以申请机构名称来确认,但某些情况(如公司所有权变更)有时会导致难以确认申请机构。FDA认为,在持续文档审查和与公司沟通的基础上,橙皮书上的申请机构名称大多数情况下是正确的。
要使药品标示上的公司名称信息与橙皮书保持一致,应注意:申请机构名称始终出现在橙皮书中。这用于确定申请机构(申请的FDA 356h表单中的公司名称)是否为经销商(标示中的大写公司名称)。然而,申请机构名称可能不会始终出现在药品的标示中。
如果申请机构是经销商,其名称出现在橙皮书和标示中;如果申请机构不是经销商,并且FDA意识到申请机构与经销商之间的合作关系(如母公司与子公司),申请机构名称出现在橙皮书中且两者的公司名称可能同时出现在标示中。存在已知合作关系的公司会出现在附录B中。如果申请机构和经销商之间不存在已知合作关系,则申请机构名称出现在橙皮书中。然而,除非申请机构是制造商、包装商或经销商,否则申请机构名称可能不会出现在标示中。该情形下,从业者将无法仅靠标示来判断上市销售的药品与橙皮书中记载的申请机构之间的关系,以及与某个特定的获批药品的关系。此种情况下,要确保讨论中的药品是获批申请的主体,应该与标示中出现的公司进行联系。
要使药品标示中的商品名称(商品名)信息与橙皮书保持一致时,应注意下列事项:如果申请机构是经销商,其名称出现在橙皮书和标示中;如果FDA意识到申请机构和经销商之间的合作关系,则药品(无商品名时则以确定的药物名称代替)的商品名称(商品名)出现在橙皮书中。如果申请所有者与经销商之间存在合作关系且两者均销售该药品,则FDA保留选择经销商或申请所有者的商品名称出现在橙皮书中的权利。如果申请机构与经销商之间不存在已知合作关系,则确定的药物名称出现在橙皮书中。
橙皮书中的每个药品任何时候均是监管的对象。可能会不时发现获批药品违反法案的一项或多项规定。此种情形下,FDA会采取适当的强制行为以纠正违法现象,必要时会通过自愿撤回、没收或其他强制行为确保从市场上取缔此类药品。然而,此类监管行为不影响橙皮书中的药品收纳。衡量药品收纳的主要标准是该药品的批准申请有效且该申请从未因安全性或有效性而被撤回。FDA相信,橙皮书保留违规药品将不会产生明显的负面健康问题,因为FDA有其他司法机制以阻止该药品的上市销售。如果因情况变化致使药品违规或FDA对是否药品达到治疗等效性标准的评价数据产生怀疑,FDA也可能变更药品的治疗等效性等级。
治疗等效性评价的代码系统的制定目的是,允许用户快速确定是否FDA已将某个特定获批药品评价为与其他药物等效药剂具有治疗等效性(第一个字母),并提供基于FDA评价基础的额外信息(第二个字母)。除少数特殊情形外,治疗等效性的评价日期与批准日期保持一致。
第一个字母代表归纳多源药品的两个基本类别,如下所示:
AFDA认为与其他药物等效药剂具有治疗等效性的药品,如下所示:
(1)不存在已知或可疑的生物等效性问题。根据剂型,此类药品分别被指定为AA、AN、AO、AP或AT;或者
(2)由充分的体内和/或体外证据证明其实际或潜在生物等效性问题已得以解决。此类药品被指定为AB。
BFDA认为当前与其他药物等效药剂不具有治疗等效性的药品,如:
尚未有充分的生物等效性证据证明其实际或潜在生物等效性问题已得以解决的药品。通常存在特定剂型的问题,而非活性成分的问题。此类药品分别被指定为BC、BD、BE、BN、BP、BR、BS、BT、BX或B*。
根据以下定义和原则,单体药品已被评价为与参比药物具有治疗等效性:
被视为与其他药物等效药剂具有治疗等效性的药品。
“A”类药品指的是那些由充分的体内和/或体外证据证明其实际或潜在生物等效性问题已得以解决的药品。被指定为代码“A”的药品满足下列主要原则之一:
(1) 对于那些未存在已知或受质疑的体外生物等效性问题的活性成分或剂型,基于一些剂型(如溶液)的其他申请数据或通过证明达到可接受的体外分解标准,满足了固体口服剂型的要求,治疗等效药剂的生物等效性所需的信息被假定或被视为是不证自明的。只要药品根据《现行优良制造规范》的条例制造而成,并且满足其获批申请的其他要求,治疗等效性等级将被指定给此类药品(根据下列记载的剂型,此类药品分别被指定为AA, AN,AO,AP或AT);或者
(2) 对于那些包含被FDA认定为活动成份或剂型存在实际或潜在生物等效性问题的DESI药品以及剂型存在潜在生物等效性问题的1962年之后的药品,仅在该获批药品通过体内体内和/或体外体外研究的充分科学依据被确定为与参比药物具有生物等效性时,治疗等效性的评价将被指定为药物等效药剂(此类药品被定义为AB)。
有一些基本准则可能会在具体的案例上影响这些治疗等效药剂。药品的处方医师和药剂师应该对这些准则提高警惕,以便于更适当地处理那些需要专业判断和裁量的情况。
生物等效药剂可能会存在标示差异,这就需要健康专家的注意。例如,根据重制后的失效日期或贮藏条件,配药时被重制成口服或注射液体的治疗等效性药粉可能会产生差异。仅在每种药品均依照该药品的标示定义的条件进行重制、贮藏及使用时,FDA评价此类药品为治疗等效药剂。
FDA将会在橙皮书中使用便签以标示一些特殊情况,如两种被评价为生物等效药剂或治疗等效药剂的药品的潜在差异,这些差异应该引起健康专家的注意。这些便签包含在“1.8章特殊情形”中。
例如,少数情况下,治疗等效药品根据其使用及给药情况可能会存在差异。这些差异可能源于使用时涉及到的专利或独占权。FDA认为该差异可能会影响到健康专家配给或更换药剂时,该便签将会添加到1.8章。
另外,参比药物可能在获批后发生变化(如用药间隔的变化),从而对FDA评价为与该药品具有治疗等效性的获批仿制药的可替代性产生影响。FDA认为参比药物的变化对治疗等效性产生了明显影响时,FDA将会变更该药品的其他仿制药的治疗等效性等级,除非这些仿制药制造商能够提供额外信息以保证其药品在该变化条件下仍具有等效性。接收到这些未审查的额外信息时,FDA可能会在1.8章中添加便签,甚至在极少数情况下会变更其治疗等效性等级。
在某些情况下(如塑料容器包装的Isolyte® SW/葡萄糖5%、塑料容器包装的Plasma-Lyte® 148与葡萄糖5%),具有紧密关系的药品会被列为包含相同的活性成分,但在数量上稍有不同。在决定哪些药品为治疗等效药剂时,FDA将那些成分的标示规格变化不超过1%的药品视为治疗等效药剂。
相同治疗配基的不同盐分和酯分将被视为药物替代品。基于橙皮书的主旨,此类药品不会被视为治疗等效药剂。在橙皮书中将不会对替代药品进行治疗等效性方面的评价或编码。无水化合物、水化合物以及不同的晶型均被视为具有治疗等效性且必须达到相同标准,必要时,氨苄青霉素/水合氨苄青霉素的等效性由适当的生物利用度/生物等效性研究进行证明。
橙皮书中的代码并不旨在妨碍保健专家使用已知的专业经验将不同浓度的药物转换为药物等效药剂。
尽管包装尺寸类型有治疗提示,但此类包装的药品并不等同于药物等效药剂。例如,一些口服避孕药提供21片包装和28片包装;28片包装中包含7片安慰片剂或含铁片剂。这两种包装药品不会被视为治疗等效药剂,因此它们也不被视为药物等效药剂。
一些药物等效药剂中的防腐剂可能会不同。防腐剂与其他非活性成分不会影响FDA的药物等效性评价,除非这些成分可能会影响生物等效性或给药途径。
那些被评价为具有药物等效性的药品的具体子码以及这些子码的定义原则如下所示:
AA传统剂型且未出现生物等效性问题的药品
药品代码为AA的药品中包含的活性成分与剂型并未出现实际或潜在生物等效性问题、药品质量或标准问题。但是,所有口服剂型必须符合适当的体外生物等效性标准,以达到FDA的接受标准并获得批准。
AB, AB1, AB2, AB3...满足所需生物等效性要求的药品
已提交证明其生物等效性的研究,且具有相同类目(如同一活性成分、剂型、给药途径)及同种类目下指定的相同规格(参阅“1.2章 治疗等效性相关术语药物等效药剂”)的多源药品通常被编码为AB。
在特定情况下,1位数字将会添加至AB代码的末尾以组成3位字符(如AB1、AB2、AB3等)。仅在同种类目下指定了一种以上的相同规格的参比药物时,3位字符代码将会被分配。仅当存在至少两种以上不具有生物等效性的药品时,通常会选择两种或两种以上参比药物。如果研究显示该药品与特定参比药物具有生物等效性,则该仿制药将被赋予与参比药物相同的3位字符代码。例如,Adalat® CC(迈尔斯)及Procardia XL®(辉瑞)的缓释片剂均被归属于活性成分硝苯地平。这些列于同一类目下的药品彼此不具有生物等效性。由FDA判断与Adalat® CC及Procardia XL®具有生物等效性的仿制药已经获得批准,Adalat® CC与Procardia XL®已分别被指定为AB1与AB2等级。与Adalat® CC具有生物等效性的仿制药将被指定为AB1等级,同时那些与Procardia XL®具有生物等效性的仿制药将被指定为AB2等级。(将某一种药品指定为AB1或AB2并不意味着药品偏好。)尽管经销商和/或再包装者的药品不在此列,但如果该申请所有者的药品被评为AB或具有3位字符代码或是该列表的单一源,则这些药品将被视为与申请所有者的药品具有治疗等效性。拥有相同类目且代码为AB的药品仅与其他相同条件的药品有治疗等效性。拥有相同类目且代码为3位字符的药品仅与其他相同条件的药品具有治疗等效性。
AN用于烟雾化作用的溶液和药粉
烟雾化药品的药物等效性的不稳定性主要是缘于不同的药品投放系统。在各种投放系统中上市使用的、用于烟雾化作用的溶液和药粉均被视为具有药物等效性和治疗等效性,并被编码为AN。那些仅在特定投放系统的药品或那些仅在特定投放系统包装的药品被编码为BN,除非它们达到适当的生物等效性标准。如果该生物等效性符合体外方法论,则特定投放系统的溶液或悬浊液将被编码为AN,如果生物等效性需要由体内方法论进行验证,则此类药品将被编码为AB。
AO可注射的油性溶液
可注射的(不经肠道的)油性溶液药品的吸收可根据作为介质的油的类型以及活性成分的浓度而持续发生变化。仅当溶液的活性成分、浓度及作为介质的油的类型全部一致时,可注射的油性溶液被视为药物等效药剂及治疗等效药剂。
AP可注射的含水溶液以及特定情况下的无水静脉注射溶液
需要注意的是,即使特定列表中的可注射(不经肠道的)药品可能被评定为具有治疗等效性,这些归属于通用类别(可注射、注射液)的药品中也可能存在重大差异。例如,一些具有治疗等效性的可注射药品被标示为不同的给药途径。另外,一些具有治疗等效性的药品可能使用不同的防腐剂或根本没有使用防腐剂。用于重制的干粉型可注射药品、浓缩型无菌稀释溶液或无菌注射溶液均为药物等效药剂。即使这些药物等效药剂被设计为优先产生相同浓度而非用于注射,且做了相似标示,它们也不会被评为相互具有治疗等效性(AP)。要与熟知的专业经验保持一致,处方医师、药剂师或个体给药者有责任熟悉该药品的标示,以确保该药品仅以标示上记载的给药途径进行开药。
特定常用大剂量玻璃容器装静脉药品未包含在橙皮书中(例如,葡萄糖注射液5%、葡萄糖注射液10%、葡萄糖氯化钠注射液0.9%),缘于这些药品为非FDA批准的市场销售药品且FDA未在简化新药申请中公布此类治疗药品的市场销售条件。这些药品包装在塑料容器中时,FDA法规需要批准申请而优于市场销售。此时批准取决于其他事项中关于该药品的特定塑料成分的已知安全信息。不管是玻璃包装或塑料包装,所有的大剂量治疗药品均需在相同标准下生产而成。因此,FDA有理由认为具有药物等效性的大剂量治疗药品的包装容器不会影响到它们的治疗等效性。
不经肠道药品的规格代表该容器的总药品含量。迄今为止,橙皮书中的不经肠道的液体药品的规格尚未公布。橙皮书中的不经肠道的液体药品的浓度单位为xmg/ml。容器中的干粉或冻干粉数量始终被认定为该药品规格。
Waxman-Hatch法案定义了参比药物的每个规格,该法案生效后,明确了橙皮书中的规格需要进行变更以反映不经肠道的溶液的规格。最终,OGD已经开始公布所有新批准的不经肠道的溶液的规格。以前我们仅公布某种已批准的不经肠道的溶液的浓度(如50mg/ml)。如果该药品有20ml和60ml两种获批容器,则这两种药品规格会显示为1Gm/20ml(50mg/ml)和3Gm/60ml(50mg/ml)。
AT局部用药
市场上有各种不同的用于皮肤病、眼部疾病、耳部疾病、肠胃疾病以及泌尿疾病的局部用药,包括药膏、凝胶、药水、药油、软膏、药泥、溶液、喷雾剂及坐药。尽管不同的局部用药可能包含相同的活性成分和效力,但这些剂型并不被视为药物等效药剂。因此,它们也不会被视为治疗等效药剂。所有包含相同活性成分且局部剂型相同的溶液和DESI药品均被视为治疗等效药剂,其中包括放弃体内生物等效性已获许可的药品以及通过化学和制造程序已充分证明其生物等效性的药品,它们均被编码为AT。
具有生物等效性问题的药物等效局部用药(包括所有1962年之后的非溶液类局部用药)存在充分的生物等效性数据时,它们被编码为AB,缺乏此类数据时,则被编码为BT。
FDA目前认为与其他药物等效药剂不具有治疗等效性的药品。
由充分生物等效性证据证明尚未解决其实际或潜在生物等效性问题的“B”药品通常存在特定剂型的问题,而非活性成分的问题。带有“B”代码的药品满足下列三个主要原则之一:
(1) 此类药品包含的活性成分或生产剂型由FDA认定具有明文记载的生物等效性问题或类似明显潜在问题,或未将表明其生物等效性的充分研究数据提交给FDA;或者
(2) 其质量标准不准确或FDA未获取足够的依据以确定其治疗等效性;或者
(3) 此类药品正处于监管审查状态。
“B”子码的具体代码定义及原则如下所示:
B*需要接受FDA的进一步调查和审查以确定其治疗等效性的药品
FDA收到药品在治疗等效性方面存在明显问题的新信息,而且仅可由FDA对申请机构提交的数据及信息进行进一步的调查和/或审查方能解决时,代码B*将被分配给那些此前定义为A或B代码的药品。B*代码代表FDA对此类药品的治疗等效性不持任何观点,直到FDA完成其调查和审查。
BC延释剂(胶囊、注射液及片剂)
缓释片剂配制成一种特定方式以使所包含药物在消化后仍能维持一定的时间。
尽管此类药剂的生物利用度研究已经得以实施,它们仍可能存在生物利用度的差异,主要是因为那些开发具有相同活性成分的缓释药品的企业很少使用相同的配方研究。因此,FDA认为同一规格且活性成分相同的缓释剂不具有治疗等效性,除非个体药品在比率及程度方面的等效性已通过充分的生物等效性研究得以明确证明。未提交生物等效性数据的缓释药品被编码为BC,而那些提交了此类数据的药品被编码为AB。
BD活性成分及剂型存在明文记载的生物等效性问题的药品
BD代码代表具有已知生物等效性问题的活性成分的药品、以及未将充分研究数据提交给FDA以证明其生物等效性的药品。而那些已经提交生物等效性研究数据的药品则被编码为AB。
BE延释口服药剂
药品可能会被胃液破坏或因之而失效,或药品可能会刺激胃粘膜时,则需要使用“肠”衣。此类包衣旨在延迟药物的释放,直到片剂通过胃。包含相同活性成分的延释剂在吸收方面存在显著性差异。除非有明确记载,FDA认为包含相同活性成分的不同延释剂存在潜在生物等效性问题,如果缺乏证明其生物等效性的体内研究,FDA将此类药品编码为BE。如果充分的体内研究已证明特定延释剂的生物等效性,则此类药品被编码为AB。
BN气溶喷雾器药物传输系统中的药品
此代码代表那种仅作为某种特定的药物传输系统的一部分或配套药品而在市场销售的药物溶液或药粉。
例如,该类型的不同药品可能会在药量及颗粒大小方面存在显著性差异。因此,FDA认为同一规格且包含相同活性成分的不同计量的气溶药剂不具有治疗等效性,除非此类药品达到适当的生物等效性标准,此类药品被编码为AB。
BP活性成分及剂型存在潜在生物等效性问题的药品
FDA的生物等效性法规(21CFR 320.33)包含标准和程序以确定特定剂型的特定活性成分是否会引起潜在生物等效性问题。FDA的原则就是,即使未有明确数据证明其非等效性,只要活性成分达到这些标准即意味着此类药品存在潜在生物等效性问题。包含此类活性成分的药物等效药剂的口服药剂被编码为BP,而提供明确体内生物等效性数据的药品被编码为AB。包含悬浮在含水或含油介质中的活性成分的可注射悬浊液也被编码为BP。可注射悬浊液会引发生物等效性问题,原因在于悬浮活性成分或悬浊液配方在颗粒大小、多形结构方面的区别均可明显影响其释放率和吸收率。未有充分生物等效性证据时,FDA认为此类药品的药物等效药剂不具有生物等效性,因此此类药品被编码为AB。
BR用于系统吸收的坐药或灌肠剂
那些旨在产生系统疗效(区别于用于个体疗效的坐药)的坐药或灌肠剂中的活性成分的吸收可因药品而明显不同。因此FDA认为仅在提供了生物等效性的体内证据时,药物等效性系统坐药或灌肠剂才具有生物等效性。提供了体内证据时,此类药品被编码为AB。未提供此类证据时,则此类药品被编码为BR。
BS缺乏药物标准的药品
如果FDA发现某种特定剂型活性成分缺乏药物标准且妨碍到FDA对药物等效性或治疗等效性作出评价时,包含该剂型活性成分的所有此类药品均被编码为BS。例如,该标准允许活性成分的多种药理有效成分,且其药物等效性处于讨论阶段,所有该剂型活性成分的药品被编码为BS。
BT存在生物等效性问题的局部用药
该代码主要代表1962年之后的皮肤病、眼部疾病、耳部疾病、肠胃疾病及泌尿疾病的局部用药,包括药膏、软膏、凝胶、药水、药泥、喷雾剂以及未作为系统药物吸收的坐药。局部用药被评价为具有不错的临床效果,但它与其他药物等效药剂不具有生物等效性或者缺乏足够的生物等效性证据,此类药品被编码为BT。
BX未有充分数据证明其治疗等效性的药品
代码BX代表特定药品,根据橙皮书中规定的原则,FDA审查的数据不足以确定其治疗等效性。在这些情况下,药品被假定为不具有治疗等效性,直到FDA确定有充分信息对其治疗等效性进行全面评价。
橙皮书中列出的特定药品的特殊情形需要进一步的讨论。特殊情形的内容如下所示:
氨基酸与水解胶原蛋白注射液。此类药品包含不同氨基酸数量及类型,因此它们不被视为药物等效药剂。鉴于此原因,这些药品并不被视为治疗等效药剂。同时,FDA认为有必要指出氮气平衡是唯一治疗目标且个体氨基酸含量不是其考虑范围,因此具有相同数量氮气的药物替代品可能被视为具有治疗等效药剂。
促卵泡素α与促卵泡素β。根据通过物理化学测试及生物测定法提取的数据判断,促卵泡素α与促卵泡素β无法辨别。
Gaviscon®。Gaviscon®是一款从1970年9月开始上市销售的非处方药。该药品的活性成分(铝氢氧化物和三硅酸镁)曾由FDA的非处方药抗酸剂专家组进行审查,并由该专家组认定为安全有效的成分(类别I)。然而,该片剂却未通过所有抗酸剂均需通过的抗酸剂测试。因此,FDA因其缺乏有效性而将该片剂划分为类别III。马里昂实验室提交了带有临床研究的全面新药申请,并于1983年12月9日由FDA批准。Gaviscon®在治疗回流酸方面的活动由其非活性成分(碳酸氢钠及海藻酸)的物理化学属性实现。因此,所有将Gaviscon®片剂作为参比药物引用的简化新药申请中都必须包含其非活性成分(碳酸氢钠及海藻酸)。要使用不同的非活性成分替代碳酸氢钠及海藻酸或者要使用这些成分中的不同结构时,需要一份全面的新药申请以证明该药品的效力。
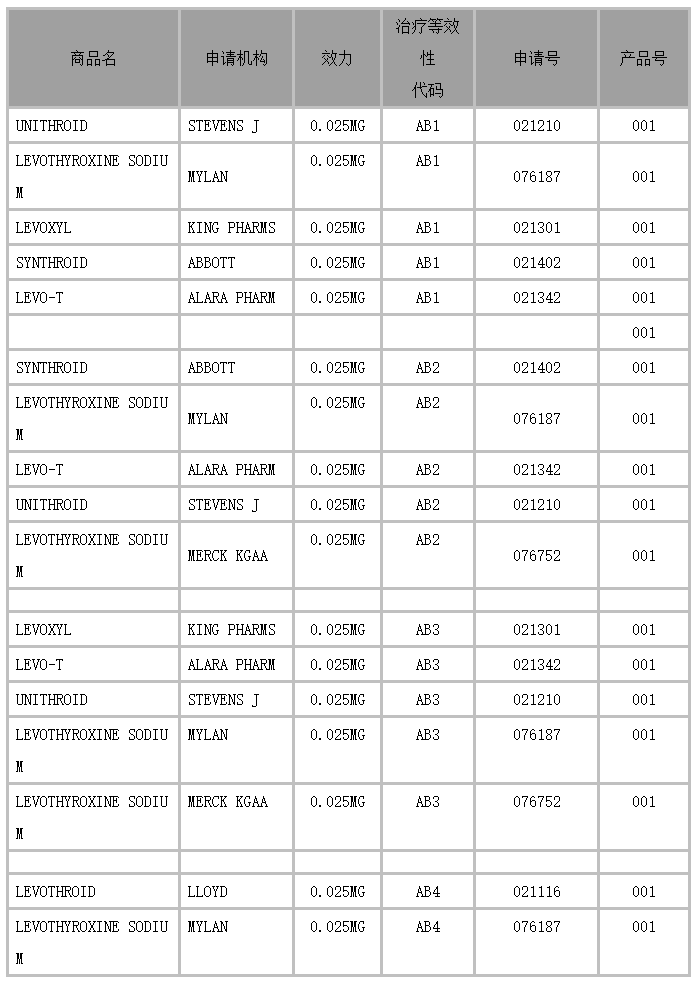
左旋甲状腺素钠。因为目前存在多种左旋甲状腺素钠的参比药物,且许多参比药物的赞助者已经开始研究与其他参比药物的治疗等效性,所以FDA确定对此类药品指定2、3个字符的治疗等效性代码的常规经验可能存在潜在矛盾且不太准确。因此,FDA为左旋甲状腺素钠药品提供下列说明及治疗等效性评价图解。
Levothyroxine Sodium(迈兰简化新药申请76187)片剂已被确定与Unithroid(Jerome Stevens新药申请021210)片剂的相应规格具有治疗等效性。
Levo-T(Alara新药申请021342)、Levothyroxine Sodium(迈兰简化新药申请76187)、Unithroid(Jerome Stevens新药申请021210)以及Levothyroxine Sodium(Merck KGAA简化新药申请76752)片剂已被确定与Synthroid(雅培新药申请021402)片剂的相应规格具有治疗等效性。
Levo-T(Alara新药申请021342)、Unithroid(Jerome Stevens新药申请021210)、LevothyroxineSodium(迈兰简化新药申请76187)以及Levothyroxine Sodium(Merck KGAA简化新药申请76752)片剂已被确定与Levoxyl(King Pharms新药申请021301)片剂的相应规格具有治疗等效性。
Levothyroxine Sodium(迈兰简化新药申请76187)片剂已被确定与Levothroid(Lloyd新药申请021116)片剂的相应规格具有治疗等效性。
本图表将所有0.025mg药品的治疗等效性代码进行简述。其他药品的规格可能比较相似。带有相同AB+数字的治疗等效性代码的药品已被确定为具有治疗等效性。一种以上的治疗等效性代码可能会适用于一些药品。通用治疗等效性代码代表药品间的治疗等效性。
专利证明 基于适当性申请的参比药物。涉及到基于适当性申请的参比药物(RLD)的简化新药申请,必须证明申请药品与参比药物具有生物等效性,并且应该包含作为已批准的适当性申请基础的参比药物的适当的专利证明及独占权声明。此观念也适用于简化新药申请,该申请引用了仍处于专利和/或独占权保护的新药申请的参比药物,如当原始参比药物的生物等效性的体外确定不证自明且放弃生物等效性的体内确定可能获得许可时,选择第二种参比药物。
放弃独占权。如果基于《联邦食品、药品及化妆品法案》(法案)的505(b)条款提交的新药申请(NDA)满足基于505(c)(3)(D)及505(j)(5)(D)条款的独占权要求,该独占权将会列在橙皮书的“专利和独占权章节”中。如果药品已经获取该独占权,FDA将会基于上述法案的505(j)条款延迟批准505(b)(2)的申请或简化新药申请(ANDA)直到该独占权失效。如果该参比药物同时被一种或多种专利保护,505(b)(2)申请或简化新药申请的批准日期取决于橙皮书中记载的专利或独占权的最新失效日期。然而,新药申请的所有者可以对涉及该受保护药品的任意或所有505(b)(2)申请和简化新药申请放弃其独占权。如果新药申请所有者放弃其独占保护权利,满足条件的505(b)(2)申请或简化新药申请可无视新药申请所有者的独占权而获得批准。新药申请所有者对所有505(b)(2)申请及简化新药申请放弃其独占权的新药申请将在橙皮书的“专利及独占权”中被编码为W,并且将引用此章节。引用该参比药物的申请机构需在独占权声明中指出该参比药物的所有者已放弃其独占权。
根据其申请或主动意愿,考虑变更已获批准的多源药品的治疗等效性代码时,FDA将会使用下列程序。FDA开始意识到新的科学信息影响到橙皮书中的整体药品分类(如关于活性成分或剂型的信息)而不是分类中单个药品的信息时,通常会进行此类变更。考虑变更特定药物实体和药剂相关的处方药目录上的所有药品的治疗等效性代码时,将会使用这些程序。可能会从表示不存在生物等效性问题的药品代码(如AA)变更为表示存在生物等效性问题的药品代码(如BP),反之亦然。该程序不适用于特定药品代码的变更(例如,从BP变更为AB或从AB变更为BX)。
在对药品的整个类别变更治疗等效性代码之前,FDA将会在积累增刊的序言中宣布正考虑进行变更并欢迎评论。评论及科学数据可发送至生物等效室的主管(MD20855 罗克韦尔市斯坦迪什办事处7620 药品评价与研究中心 仿制药事务处 HFD-610)。
评论期限通常最长为60天,并且评论的结束日期将会记载于每种药物实体的变更说明中。
最有用的科学数据类型为基于各批次主体药品的体内生物利用度/生物等效性研究。这些提交需要介绍使用的分析程序与设备的全面说明、分析方法论的类型,包括分析数据时用到的标准曲线、计算结果的方法说明、药代动力学及分析模型的说明。逸闻或推荐信信息对FDA而言没有太大用处,而且此类提交也不被推荐。然而,发布在科学文献的文档副本或未发布的资料则受欢迎
上述程序并不适用于单一药品代码的变更。例如,根据合格的生物等效性研究结果将单一药品的代码由BP变更为AB,通常不是通告和评论的主题。同样,单一药品代码从AB变更为BX(例如,存在明显生物等效性问题)不需要通告或评论。FDA的更重要的职责是将可能需要变更药品代码的治疗等效性的最新信息提供给公众,而不是提供任何正式通告和机会给申请机构。如果该撤回行动尚未实施,《联邦登记簿》中撤回药品批准的公告通常会使药品代码从AB变更为BX。
橙皮书的“停用药品章节”中的药品未因安全性或有效性而被召回时,会在药品规格下方记载“根据《联邦登记簿》的决定,该药品未因安全性或有效性而被停用或撤回”。那些药品仅是1995年之后的公民申请决定的反映。橙皮书的“停用药品章节”中的药品的认定应该避免对相同药品进行多次公司申请提交。不再适用的FR通告将从年刊中移除(例如,当前上市销售的参比药物及不再适用的专利或独占权)。FR安全性或有效性确定列表中记载了当前有通告或已移除通告的药品。该目录每季度更新一次。该年度中发布的通告将在药品生效的当月添加到电子橙皮书查询中。
通常情况下,申请所有者通知橙皮书工作人员其药品不再销售时,该获批药品将会添加到橙皮书的“停用药品章节”中。如果年度报告显示该药品已不再销售或已实施其他FDA行政行为(如撤回申请),则此类药品可能也会添加到上述章节中。橙皮书的变更不受法案的510条款的药品注册及记载要求的影响。
我们会尽最大的努力确保年刊的内容准确并保持最新状态。申请所有者被要求向FDA橙皮书工作人员(OBS)提供任何变更或修正。请在药品不再销售时通知OBS。药品已证实不再包含在下一次发布的橙皮书更新中时,必须在当月月底通知橙皮书工作人员以将此类药品添加到停用药品目录中而不是橙皮书的第1、2或3章中(已在1.1章中进行了讨论)。
可以通过电子邮件联系drugproducts@fda.hhs.gov。
通过传真发送变更至:240-276-8974;
写信至: MD 20855,罗克韦尔市,斯坦迪什办事处7620,仿制药办公室 HFD-610,FDA/CDER 橙皮书工作人员
随着第25版的发布,年刊及每月积累增刊以便携文档格式(PDF)刊载到EOB的主页电子橙皮书查询上,通过点击出版物即可获取。该PDF年度版中包括之前的纸质版,但不包括孤儿药指定及批准目录。PDF格式的年度馈赠版可从美国政府印刷办公室(866-512-1800)获取。







