本期将进行药物质量控制-特殊杂质的鉴定与检查的相关讲解。
药物中特殊杂质(或有关物质)的研究是药物质量控制的重要部分。该研究可以为药物的生产工艺优化、质量研究与控制、稳定性考察、药理毒理及临床研究等提供重要的参考依据。所以,特殊杂质研究直接体现创新药物研究的水平。
根据ICH的要求,创新药物原料和新制剂中的杂质,表观含量在0.1%及其以上的杂质,以及表观含量在0.1%以下的具强烈生物作用的杂质或毒性杂质,均要求进行定性分析、鉴定结构。这些杂质一般包括药物合成中的有机杂质和稳定性试验中的分降解产物,即药物中的有关物质。
对药物中的特殊杂质/有关物质进行定性研究具有重要意义。通过有关物质的研究与鉴定,可以获得有关物质的结构信息,分析其形成机制;

以便:① 优化生产过程(原料药的合成工艺与精制纯化条件,制剂的处方、相容性和加工工艺),尽量避免有关物质的形成;② 优化设置贮藏条件,减少分降解产物的产生。使它们的含量达到合理的限度水平要求。
即使是仿制药品,在其研制和生产过程中,也必须研究其杂质谱与原研药品的一致性。如出现新增杂质,应按上述ICH的基本要求进行全面研究,制订适宜的检查控制项目。
多组分药物中共存的异构体,或抗生素多组分,一般不作为杂质检查项目。必要时,这些共存物质可在质量标准中规定其比例,以保证原料药的质量一致性。

例如:硫酸庆大霉素中“庆大霉素C组分”(C1、CI,a、C2、C2a)相对比例的检查:C,应为25%~50%,Cu应为15%~0%,C2+Ca应为20%~50%头孢泊肟酯中“异构体”A和B的检査,在含量测定项下记录的供试品溶液色谱图中,头孢泊肟酯异构体B峰面积与头孢泊肟酯异构体A,B峰面积和之比应为0.50~0.60。
但当共存物质为毒性杂质时,该物质就不再认为是共存物质。例如,单一对映体药物中,可能共存的其他对映体,应作为杂质检査,并设置“比旋度”或“光学异构体”检查项目;对消旋体药物的质量标准,必要时,则应该设置旋光度检査项目。

药物中特殊杂质的检查分析方法应专属、灵敏。杂质检查通常应尽量采用现代色谱分离分析手段,主成分与杂质和降解产物均应有良好的分离度;其检测限应满足限度检查的要求;对于需作定量检查的杂质,方法的定量限应满足检测的灵敏度和准确度要求。检查分析方法均需按要求进行方法验证。
特殊杂质检查研究时,应采用多种不同的分离分析方法或不同测试条件,进行研究比较,并对测定结果进行比对分析。以便选择较佳的方法与条件,满足药品质量控制和标准中相应检查项目设置的要求。
特殊杂质检查分析方法的建立,应考虑普遍适用性,所用的仪器和试验材料应容易获得。对于特殊试验材料,应在质量标准明确规定。在特殊杂质分析的研究阶段,应使用可能存在的杂质、强制降解的产物,分别或加入主成分中,配制供试溶液,进行色谱条件探索、比较和优化,并建立相应的系统适用性要求,保证方法专属、灵敏、准确。
特殊杂质研究中,必要时,应进行杂质的分离纯化制备或合成制备,以供进行安全性和质量研究。对确实无法获得的杂质和降解产物,应在药物质量研究资料和药物质量标准起草说明中说明理由。
在采用现代色谱技术对特殊杂质进行分离分析的情况下,对特定杂质中的已知杂质和毒性杂质,应使用杂质对照品进行定位;无法获得对照品时,可用相对保留值进行定位;特定杂质中的未知杂质可用相对保留值进行定位。特殊杂质的含量可按照薄层色谱法(ChP2015通则0502)、高效液相色谱法(ChP2015通则0512)等方法进行测定。
对于立体异构体杂质的检测,可以采用手性的色谱或高效毛细管电泳等方法。对于立体异构体杂质检查方法的验证,应重点考察立体专属性(选择性)和潜在的手性转化行为。

通常,应尽量使立体异构体杂质的出峰顺序在主成分峰之前,以利于两者的分离和检测灵敏度的提高。另外,由于手性色谱法不能直接反映手性药物的光学活性,需要与比旋度测定相互补充,以有效控制手性药物的质量。
由于色谱法进行杂质限度检查时,受色谱参数设置值的影响较大,因此,有关操作注意事项,应在起草说明中详细阐述,必要时,可在质量标准中予以规定。
测定法(不加校正因子的主成分自身对照法):精密量取供试品溶液与对照溶液各20u1,分别注人液相色谱仪,记录色谱图。供试品溶液的色谱图中如有左旋异构体峰,其峰面积不得大于对照溶液主峰面积(1.0%)。

杂质限度的制订应考虑如下因素:
① 杂质及含一定限量杂质药品的毒理学研究结果;
② 给药途径;
③ 每日剂量;
④ 给药人群;
⑤ 杂质药理学可能的研究结果;
⑥ 原料药的来源;
⑦ 治疗周期;
⑧ 在保证安全有效的前提下,药品生产企业对生产高质量药品所需成本和消费者对药品价格的承受能力等。
在综合考虑上述因素的情况下,制订合理的限度,保障药品质量可靠、使用安全、疗效明确。尤其对于毒性杂质和毒性残留有机溶剂应严格规定限度。
大多数杂质的限度,均可以参照本章“残留溶剂的限度要求”中介绍的限度估算方法确定。

特殊杂质的研究涉及多方面协调配合,包括原料和(或)制剂的工艺过程研究、分析方法选择和开发、降解过程与产物分析和结构鉴定等。而结构鉴定或解析工作还需要分离化学和光谱测定与解析的密切配合才能有效完成。研究策略可参照工作流程图进行。
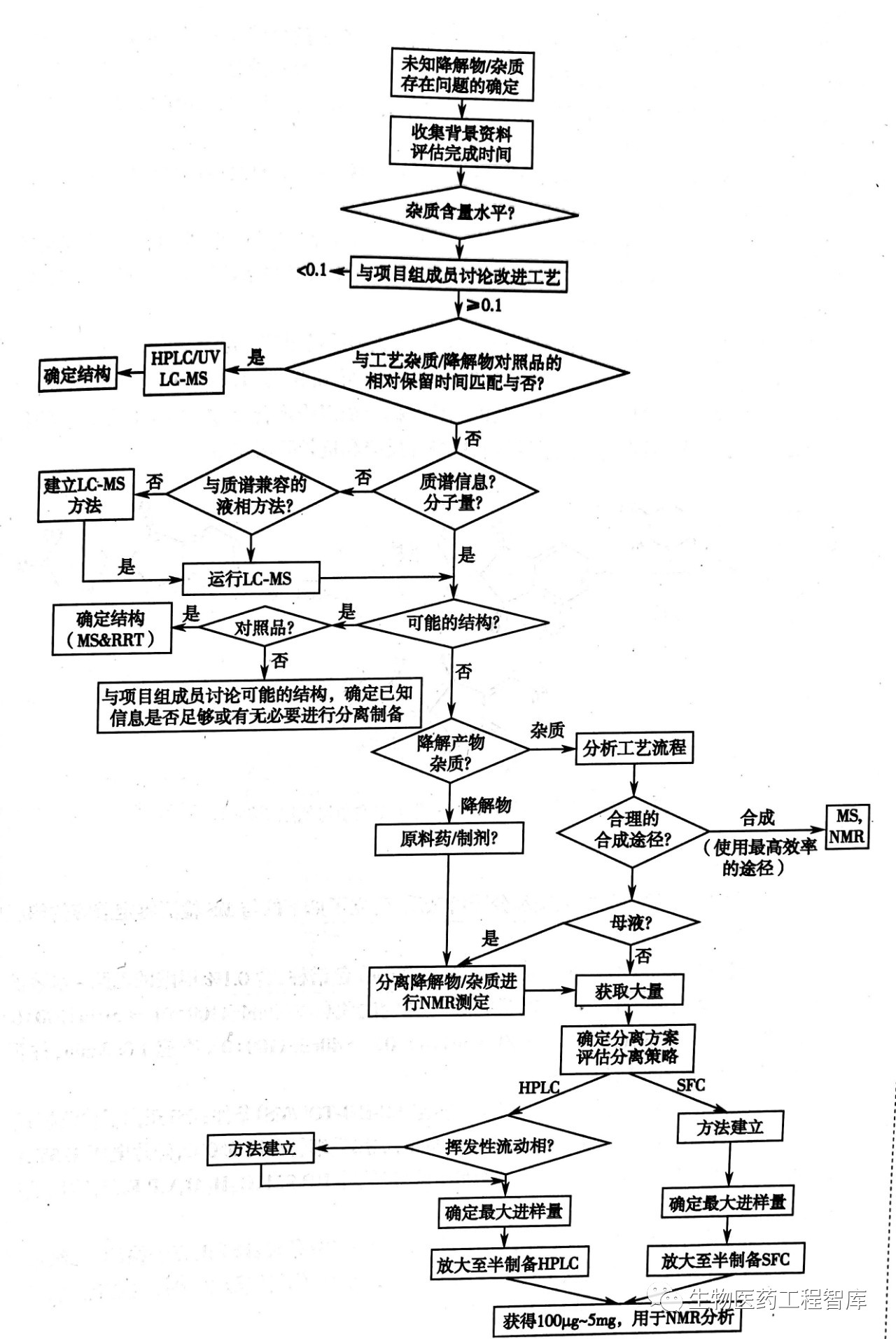
药物中的微量特殊杂质,大都首先使用现代联用技术检测和分析解析,推测其可能的结构;并结合药物的合成工艺路线、化学反应机制等,分析杂质的引人环节,推定或确证它们的结构。
当然,必要时应当尽可能制得它们的纯净对照品,进行全面的色谱和光谱测定,并解析确证它们结构。药物特殊杂质(有机杂质)的制备,通常有两种方法:分离纯化制备法和合成制备法。在获得足够量的情况下,可以对特殊杂质进一步进行安全性评价和质量控制研究,为药品质量标准指标的制定提供参考依据。
分离纯化杂质对照品法:当药物中待鉴定杂质的含量较大时,可以使用制备色谱法进行分离纯化,得到特定杂质,然后再通过色谱和光谱分析确证结构。

合成杂质对照品法:当样品中的杂质量较小,且杂质的分离纯化较为困难时,可以合成杂质对照品,通过比较杂质与对照品的色谱和光谱特征,判断杂质与对照品是否完全一致,从而确证杂质的结构。
References:
[1]《药品质量生产管理规范》2010修订版
[2]《药物分析》
作者/ 生物医药工程智库 编辑/ ZK主创们
声明:药研江湖对所有公众号产生内容保持严谨、中立的态度。文章仅供交流学习使用。如遇到内容有误,请与我们联系进行讨论和修改。(010-65104668)








